I nostri prudutti principali: silicone aminicu, silicone in blocchi, silicone idrofilu, tutta a so emulsione di silicone, miglioratore di a resistenza à u sfregamentu bagnante, idrorepellente (senza fluoru, Carboniu 6, Carboniu 8), chimichi di lavaggio smin (ABS, enzimi, protettore Spandex, rimuovitore di manganese), più dettagli cuntattate: Mandy +86 19856618619 (Whatsapp)
Introduzione à i tensioattivi
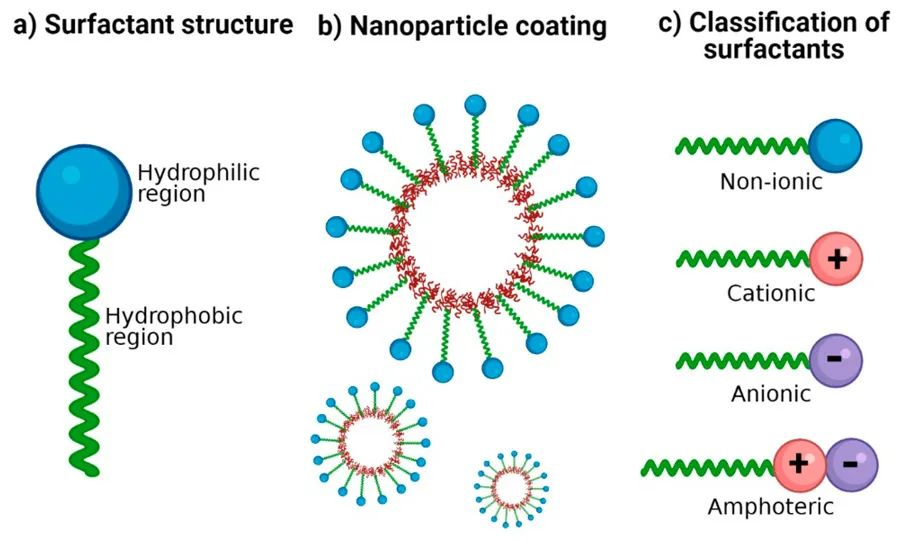
I tensioattivi pussedenu una struttura moleculare anfifilica: una estremità cuntene un gruppu idrofilu, chjamatu testa idrofila, mentre chì l'altra estremità cuntene un gruppu idrofobicu, cunnisciutu cum'è coda idrofobica. A testa idrofila permette à i tensioattivi di dissolve si in acqua in a so forma monomerica.
U gruppu idrofilu hè spessu un gruppu polare, chì pò esse un gruppu carbossile (-COOH), un gruppu d'acidu sulfonicu (-SO3H), un gruppu aminu (-NH2), amine è i so sali, gruppi idrossilici (-OH), gruppi ammidici, o ligami eterei (-O-) cum'è altri esempi di gruppi idrofilici polari.
U gruppu idrofobicu hè tipicamente una catena idrocarburica non polare, cum'è e catene alchiliche idrofobiche (R- per alchile) o i gruppi aromatichi (Ar- per arile).
I tensioattivi ponu esse classificati in tensioattivi ionichi (cumpresi i tensioattivi cationichi è anionici), tensioattivi non ionichi, tensioattivi anfoteri, tensioattivi misti è altri. In e soluzioni di tensioattivi, quandu a cuncentrazione di u tensioattivo righjunghje un certu valore, e molecule di tensioattivi formanu diversi aggregati ordinati cunnisciuti cum'è micelle. U prucessu di micellizazione, o furmazione di micelle, hè una pruprietà fundamentale cruciale di e soluzioni di tensioattivi, postu chì parechji fenomeni interfacciali impurtanti sò assuciati à a furmazione di micelle.
A cuncentrazione à a quale i tensioattivi formanu micelle in suluzione hè chjamata Cuncentrazione Micellare Critica (CMC). E micelle ùn sò micca strutture fisse è sferiche; piuttostu, mostranu una irregolarità estrema è cambiamenti di forma dinamica. In certe cundizioni, i tensioattivi ponu ancu mustrà stati micellari inversi.
Fattori chì influenzanu a CMC:
- Struttura di u tensioattivu
- Tipu è presenza di additivi
- Temperatura
Interazzione trà tensioattivi è proteine
E proteine cuntenenu gruppi non polari, polari è carichi, è parechje molecule anfifiliche ponu interagisce cù e proteine in vari modi. Sicondu e cundizioni, i tensioattivi ponu furmà aggregati urganizati molecularmente cù strutture diverse, cum'è micelle o micelle inverse, chì interagiscenu in modu diversu cù e proteine.
L'interazzione trà e proteine è i tensioattivi (Proteina-Tensioattivu, PS) implicanu principalmente interazzione elettrostatiche è interazzione idrofobiche. I tensioattivi ionichi interagiscenu cù e proteine principalmente per via di e forze elettrostatiche di u gruppu polare è di l'interazzione idrofobiche di a catena di carbone alifatica, ligandu si à e regioni polari è idrofobiche di a proteina, furmendu cusì cumplessu di PS.
I tensioattivi non ionichi interagiscenu principalmente cù e proteine per via di forze idrofobiche, induve e catene idrofobiche interagiscenu cù e regioni idrofobiche di e proteine. L'interazione pò influenzà sia a struttura sia a funzione di u tensioattivo è di a proteina. Dunque, u tipu è a cuncentrazione di tensioattivi, inseme cù u cuntestu ambientale, determinanu se i tensioattivi stabilizanu o destabilizzanu e proteine, è ancu se prumove l'aggregazione o a dispersione.
Valore HLB di i tensioattivi
Per chì un tensioattivu mostri a so attività interfacciale unica, deve equilibrà i cumpunenti idrofobichi è idrofili. L'HLB (Equilibriu Idrofilu-Lipofilu) hè una misura di l'equilibriu idrofilu-lipofilu di i tensioattivi è serve cum'è indicatore di e proprietà idrofile è idrofobiche di i tensioattivi.
U valore HLB hè un valore relativu (chì varieghja da 0 à 40). Per esempiu, a paraffina hà un valore HLB di 0 (nisun cumpunente idrofilu), u polietilenglicole hà un valore HLB di 20, è l'SDS (dodecilsolfatu di sodiu) assai idrofilu hà un valore HLB di 40. U valore HLB pò serve cum'è riferimentu guida quandu si sceglienu i tensioattivi. Un valore HLB più altu indica una migliore idrofilicità, mentre chì un valore HLB più bassu suggerisce una idrofilicità più scarsa.
Data di publicazione: 10 settembre 2024

